Die Cyanogruppe besitzt eine hohe Polarität und Elektronenabsorptionsfähigkeit und kann daher tief in das Zielprotein eindringen, um Wasserstoffbrückenbindungen mit wichtigen Aminosäureresten im aktiven Zentrum zu bilden. Gleichzeitig ist die Cyanogruppe bioelektronisch isoster zu Carbonyl-, Halogen- und anderen funktionellen Gruppen, wodurch die Wechselwirkung zwischen kleinen Wirkstoffmolekülen und Zielproteinen verstärkt wird. Daher findet sie breite Anwendung bei der Strukturmodifikation von Arzneimitteln und Pestiziden [1]. Zu den repräsentativen cyanogruppenhaltigen Arzneimitteln gehören Saxagliptin (Abbildung 1), Verapamil, Febuxostat usw.; zu den Pflanzenschutzmitteln zählen Bromofenitril, Fipronil und weitere. Darüber hinaus besitzen Cyanoverbindungen auch in der Duftstoff- und Materialforschung wichtige Anwendungsgebiete. Beispielsweise ist Citronitril ein international anerkannter Nitrilduftstoff, und 4-Brom-2,6-difluorbenzonitril ist ein wichtiger Rohstoff für die Herstellung von Flüssigkristallmaterialien. Aufgrund ihrer einzigartigen Eigenschaften finden Cyanoverbindungen in verschiedenen Bereichen breite Anwendung [2].
Die Cyanogruppe besitzt eine hohe Polarität und Elektronenabsorptionsfähigkeit und kann daher tief in das Zielprotein eindringen, um Wasserstoffbrückenbindungen mit wichtigen Aminosäureresten im aktiven Zentrum zu bilden. Gleichzeitig ist die Cyanogruppe bioelektronisch isoster zu Carbonyl-, Halogen- und anderen funktionellen Gruppen, wodurch die Wechselwirkung zwischen kleinen Wirkstoffmolekülen und Zielproteinen verstärkt wird. Daher findet sie breite Anwendung bei der Strukturmodifikation von Arzneimitteln und Pestiziden [1]. Zu den repräsentativen cyanogruppenhaltigen Arzneimitteln gehören Saxagliptin (Abbildung 1), Verapamil, Febuxostat usw.; zu den Pflanzenschutzmitteln zählen Bromofenitril, Fipronil und weitere. Darüber hinaus besitzen Cyanoverbindungen auch in der Duftstoff- und Materialforschung wichtige Anwendungsgebiete. Beispielsweise ist Citronitril ein international anerkannter Nitrilduftstoff, und 4-Brom-2,6-difluorbenzonitril ist ein wichtiger Rohstoff für die Herstellung von Flüssigkristallmaterialien. Aufgrund ihrer einzigartigen Eigenschaften finden Cyanoverbindungen in verschiedenen Bereichen breite Anwendung [2].
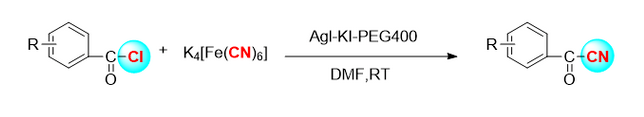
2.2 Elektrophile Cyanidierungsreaktion von Enolborid
Das Team um Kensuke Kiyokawa [4] nutzte die Cyanidreagenzien n-Cyano-n-phenyl-p-toluolsulfonamid (NCTS) und p-Toluolsulfonylcyanid (tscn) zur hocheffizienten elektrophilen Cyanidierung von Enol-Borverbindungen (Abbildung 3). Mit diesem neuen Verfahren lassen sich verschiedene β-Acetonitrile und eine breite Palette von Substraten umsetzen.
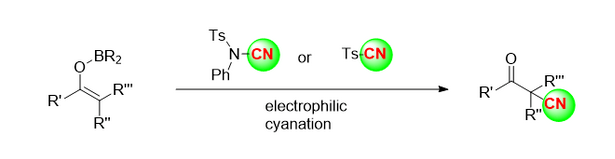
2.3 Organisch-katalytische stereoselektive Silicocyanid-Reaktion von Ketonen
Kürzlich berichtete das Team um Benjamin List [5] in der Zeitschrift Nature über die Enantiomerentrennung von 2-Butanon (Abbildung 4a) und die asymmetrische Cyanidreaktion von 2-Butanon mit Enzymen, organischen Katalysatoren und Übergangsmetallkatalysatoren unter Verwendung von HCN oder tmscn als Cyanidreagenz (Abbildung 4b). Mit tmscn als Cyanidreagenz wurden 2-Butanon und eine Vielzahl anderer Ketone unter den katalytischen Bedingungen von idpi hoch enantioselektiven Silylcyanidreaktionen unterzogen (Abbildung 4C).
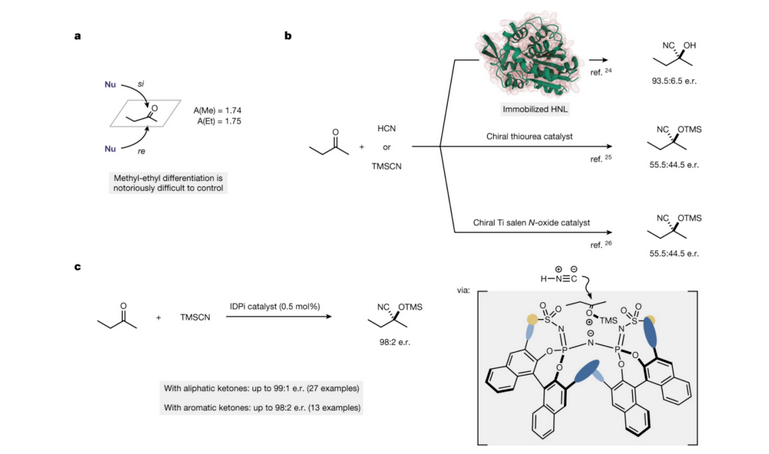
Abbildung 4 A, Enantiomerentrennung von 2-Butanon. b. Asymmetrische Cyanidierung von 2-Butanon mit Enzymen, organischen Katalysatoren und Übergangsmetallkatalysatoren.
c. Idpi katalysiert die hoch enantioselektive Silylcyanid-Reaktion von 2-Butanon und einer breiten Palette anderer Ketone.
2.4 Reduktive Cyanidierung von Aldehyden
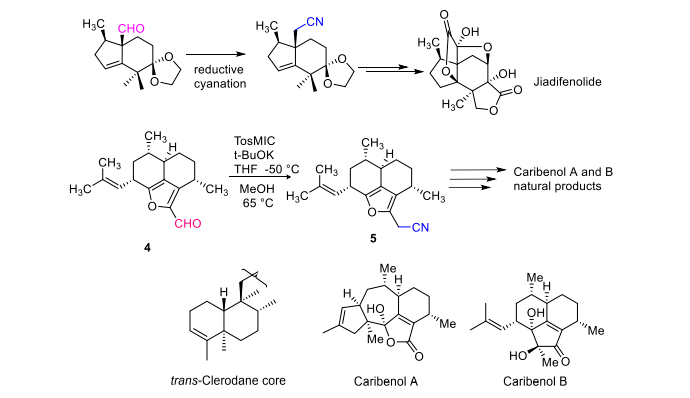
Bei der Synthese von Naturstoffen wird das grüne Tosmic als Cyanidreagenz eingesetzt, um sterisch anspruchsvolle Aldehyde leicht in Nitrile umzuwandeln. Mit dieser Methode lässt sich außerdem ein zusätzliches Kohlenstoffatom in Aldehyde und Ketone einführen. Sie ist von konstruktiver Bedeutung für die enantioselektive Totalsynthese von Jiadifenolid und ein Schlüsselschritt in der Synthese von Naturstoffen wie Clerodan, Caribenol A und Caribenol B [6] (Abbildung 5).
2.5 Elektrochemische Cyanidreaktion von organischen Aminen
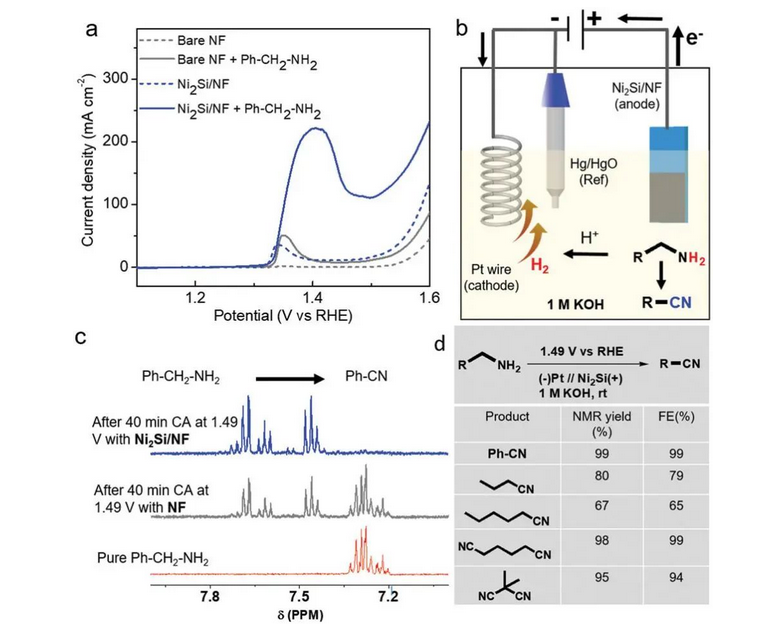
Als umweltfreundliche Synthesetechnologie findet die organische elektrochemische Synthese breite Anwendung in verschiedenen Bereichen der organischen Synthese. In den letzten Jahren hat sie zunehmend an Bedeutung gewonnen. Das Team um Prashanth W. Menezes [7] berichtete kürzlich, dass aromatische oder aliphatische Amine in 1 M KOH-Lösung (ohne Zugabe von Cyanid) bei einem konstanten Potential von 1,49 Vrhe mit Hilfe des kostengünstigen Ni2Si-Katalysators direkt und mit hoher Ausbeute zu den entsprechenden Cyanoverbindungen oxidiert werden können (Abbildung 6).
03 Zusammenfassung
Die Cyanidierung ist eine sehr wichtige Reaktion in der organischen Synthese. Ausgehend von den Prinzipien der grünen Chemie werden umweltfreundliche Cyanidreagenzien anstelle der traditionellen, toxischen und schädlichen Cyanidreagenzien eingesetzt. Neue Methoden wie lösungsmittelfreie, nicht-katalytische und Mikrowellenbestrahlungsverfahren erweitern den Forschungsbereich und die Forschungstiefe und versprechen so erhebliche wirtschaftliche, soziale und ökologische Vorteile in der industriellen Produktion [8]. Mit dem kontinuierlichen Fortschritt der wissenschaftlichen Forschung wird sich die Cyanidreaktion hin zu höherer Ausbeute, Wirtschaftlichkeit und den Prinzipien der grünen Chemie weiterentwickeln.
Veröffentlichungsdatum: 07.09.2022





